一、全國(guó)醫(yī)療器械不良事件報(bào)告總體情況
2013年,全國(guó)醫(yī)療器械不良事件報(bào)告工作呈現(xiàn)良好的發(fā)展態(tài)勢(shì)。報(bào)告數(shù)量持續(xù)增長(zhǎng),已突破23萬(wàn)份,平均百萬(wàn)人口報(bào)告數(shù)已達(dá)179份;不良事件報(bào)告的整體質(zhì)量有所提升;各地對(duì)不良事件報(bào)告的重視程度明顯提高。
(一)2013年可疑不良事件報(bào)告數(shù)量
2013年,國(guó)家藥品不良反應(yīng)監(jiān)測(cè)中心共收到《可疑醫(yī)療器械不良事件報(bào)告表》238,650份,與2012年相比增長(zhǎng)31.7%。企業(yè)后續(xù)提交《醫(yī)療器械不良事件補(bǔ)充報(bào)告表》705份;《醫(yī)療器械不良事件年度匯總報(bào)告表》1,805份(表1)。
表1 2013年可疑不良事件報(bào)告數(shù)量與2012年比較情況
| 報(bào)告類型 |
報(bào)告數(shù)量 |
年度增長(zhǎng)率(%) |
|
| 2012年 |
2013年 |
||
| 《可疑醫(yī)療器械不良事件報(bào)告表》 (《醫(yī)療器械不良事件補(bǔ)充報(bào)告表》) |
181255 (634) |
238650 (705) |
31.7 (11.2) |
| 《醫(yī)療器械不良事件年度匯總報(bào)告表》 |
1381 |
1805 |
30.7 |
1.死亡及嚴(yán)重傷害事件報(bào)告數(shù)量
2013年,國(guó)家藥品不良反應(yīng)監(jiān)測(cè)中心共收到死亡不良事件報(bào)告75份,嚴(yán)重傷害事件報(bào)告34,524份,共計(jì)34,599份,占可疑不良事件報(bào)告總數(shù)的百分比為14.5%,比2012年的23,548份增長(zhǎng)了46.9%。(圖1)。

圖1 2012-2013年全國(guó)死亡及嚴(yán)重傷害事件報(bào)告數(shù)比較
2.補(bǔ)充報(bào)告數(shù)量
2013年,國(guó)家藥品不良反應(yīng)監(jiān)測(cè)中心共收到醫(yī)療器械不良事件補(bǔ)充報(bào)告705份,年度增長(zhǎng)率11.2%,相對(duì)于死亡及嚴(yán)重傷害事件報(bào)告的快速增長(zhǎng),承載更多信息的補(bǔ)充報(bào)告數(shù)量增長(zhǎng)緩慢,說(shuō)明生產(chǎn)企業(yè)作為報(bào)告主體的主動(dòng)性不夠。各級(jí)監(jiān)測(cè)機(jī)構(gòu)對(duì)生產(chǎn)企業(yè)的督促還需加強(qiáng),在監(jiān)管同時(shí)加大技術(shù)指導(dǎo)力度,幫助企業(yè)做好監(jiān)測(cè)和報(bào)告工作。(圖2)。
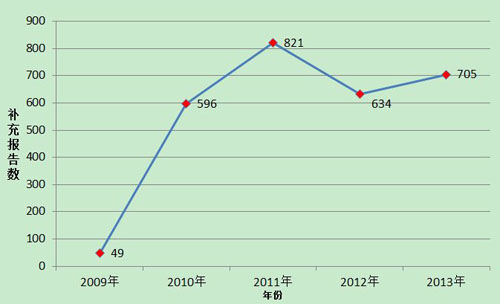
圖2 2009-2013年全國(guó)醫(yī)療器械不良事件補(bǔ)充報(bào)告數(shù)量
3.年度匯總報(bào)告數(shù)量
按照《醫(yī)療器械不良事件監(jiān)測(cè)和再評(píng)價(jià)管理辦法(試行)》的要求,第二、三類醫(yī)療器械生產(chǎn)企業(yè)應(yīng)當(dāng)在每年1月底前對(duì)上一年度醫(yī)療器械不良事件監(jiān)測(cè)情況進(jìn)行匯總分析,并填寫《醫(yī)療器械不良事件年度匯總報(bào)告表》,報(bào)所在地省、自治區(qū)、直轄市醫(yī)療器械不良事件監(jiān)測(cè)技術(shù)機(jī)構(gòu)。
2013年,國(guó)家藥品不良反應(yīng)監(jiān)測(cè)中心共收到醫(yī)療器械不良事件年度匯總報(bào)告1,805份,僅占全國(guó)現(xiàn)有的二、三類醫(yī)療器械生產(chǎn)企業(yè)數(shù)量(二類8,255家,三類2,513家)的16.8%。
4.每百萬(wàn)人口平均報(bào)告數(shù)量
2013年,我國(guó)每百萬(wàn)人口平均可疑醫(yī)療器械不良事件報(bào)告數(shù)為179份,已經(jīng)達(dá)到并超過(guò)《國(guó)家藥品安全“十二五”規(guī)劃》中100份/百萬(wàn)人的要求,但各省間發(fā)展不平衡,還有1/3的省份百萬(wàn)人口報(bào)告數(shù)偏低。2013年百萬(wàn)人口平均報(bào)告數(shù)與2012年相比增長(zhǎng)了30.7%,與2011年相比增長(zhǎng)了94.6%。較之報(bào)告總數(shù)的增長(zhǎng),百萬(wàn)人口報(bào)告數(shù)可更好地反映報(bào)告數(shù)量的增長(zhǎng)情況(圖3)。
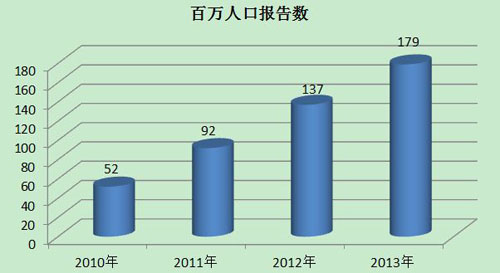
圖3 2010-2013年全國(guó)百萬(wàn)人口報(bào)告數(shù)量比較
5.注冊(cè)基層用戶數(shù)量
截止到2013年12月31日,在全國(guó)醫(yī)療器械不良事件監(jiān)測(cè)系統(tǒng)中,注冊(cè)基層用戶(包括生產(chǎn)企業(yè)、經(jīng)營(yíng)企業(yè)和使用單位)共148,585家。其中,醫(yī)療器械生產(chǎn)企業(yè)8,495家,約占注冊(cè)基層用戶總數(shù)的5.7%;經(jīng)營(yíng)企業(yè)61,498家,約占注冊(cè)基層用戶的41.4%;使用單位78,592家,約占注冊(cè)基層用戶的52.9%(圖4)。
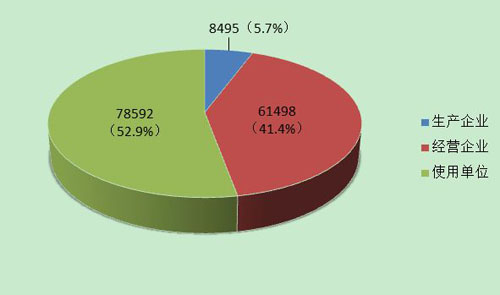
圖4 2013年全國(guó)醫(yī)療器械不良事件監(jiān)測(cè)系統(tǒng)基層用戶注冊(cè)情況
2013年,在148,585家注冊(cè)基層用戶中,提交過(guò)報(bào)告的單位數(shù)量為31,505家,占21.2%,基層用戶上報(bào)情況詳見(jiàn)表2。
表2 基層用戶上報(bào)報(bào)告情況
| 基層用戶 |
注冊(cè)數(shù) |
上報(bào)報(bào)告的單位數(shù)量 |
百分比(%) |
|||
| 總數(shù) |
可疑醫(yī)療器械 不良事件報(bào)告 |
醫(yī)療器械不良 事件補(bǔ)充報(bào)告 |
醫(yī)療器械不良 事件年度匯總報(bào)告 |
|||
| 經(jīng)營(yíng)企業(yè) |
61498 |
9576 |
9576 |
0 |
0 |
15.6 |
| 使用單位 |
78592 |
19335 |
19335 |
0 |
0 |
24.6 |
| 生產(chǎn)企業(yè) |
8495 |
2594 |
975 |
77 |
1805 |
30.5 |
| 合計(jì) |
148585 |
31505 |
29886 |
77 |
1805 |
21.2 |
(二)2002年至2013年全國(guó)可疑不良事件報(bào)告總數(shù)量
2002年1月1日至2013年12月31日,國(guó)家藥品不良反應(yīng)監(jiān)測(cè)中心累計(jì)收到《可疑醫(yī)療器械不良事件報(bào)告表》735,559份(圖5)。
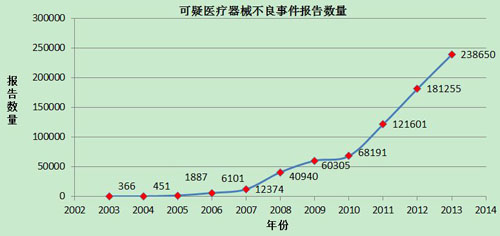
圖5 2002-2013年全國(guó)可疑醫(yī)療器械不良事件報(bào)告數(shù)量
二、醫(yī)療器械不良事件報(bào)告統(tǒng)計(jì)分析
(一)按報(bào)告來(lái)源統(tǒng)計(jì)分析
2013年醫(yī)療器械不良事件報(bào)告中,使用單位上報(bào)175,317份,占報(bào)告總數(shù)的73.5%;生產(chǎn)企業(yè)上報(bào)7,274份,占報(bào)告總數(shù)的3.1%;經(jīng)營(yíng)企業(yè)上報(bào)52,736份,占報(bào)告總數(shù)的22.1%;還有3,323份報(bào)告來(lái)自于個(gè)人,占報(bào)告總數(shù)的1.4%(圖6)。
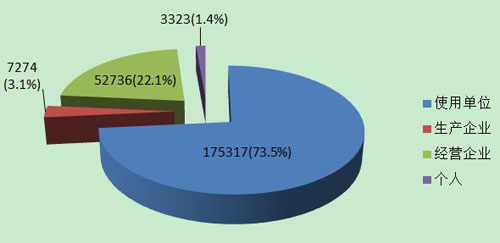
圖6 2013年醫(yī)療器械不良事件報(bào)告來(lái)源
總體來(lái)看,來(lái)自于使用單位的報(bào)告較多,來(lái)自于生產(chǎn)企業(yè)的報(bào)告較少。相比2012年,生產(chǎn)企業(yè)的報(bào)告數(shù)絕對(duì)值及所占的百分比都有所上升,但仍與其第一責(zé)任人的地位不符。提示生產(chǎn)企業(yè)履行職責(zé)的自覺(jué)性還有待進(jìn)一步提高。經(jīng)營(yíng)企業(yè)報(bào)告所占的百分比由2012年的21.58%上升至22.1%。
2013年,注冊(cè)基層用戶數(shù)量達(dá)到148,585,比2012年增加71.4%。但上報(bào)不良事件報(bào)告的單位所占比例與去年基本持平。在所有注冊(cè)的基層用戶中,僅有21.2%的用戶提交過(guò)不良事件報(bào)告。其中,經(jīng)營(yíng)企業(yè)的上報(bào)比例最低,注冊(cè)的61,498家用戶中有9,576家提交了報(bào)告,僅占15.6%;生產(chǎn)企業(yè)注冊(cè)的8,495家用戶中有2,594家提交了報(bào)告,占30.5%;使用單位注冊(cè)的78,592家用戶中有19,335家提交了報(bào)告,占24.6%。盡管注冊(cè)基層用戶的數(shù)量大幅增加,但用戶提交報(bào)告比例偏低,提示對(duì)基層用戶的宣傳培訓(xùn)、督促檢查工作還需要進(jìn)一步加強(qiáng)(圖7)。
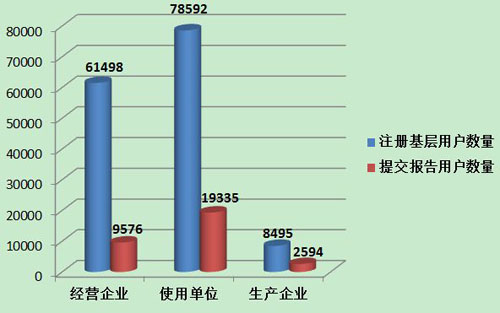
圖7 2013年注冊(cè)基層用戶提交報(bào)告情況
(二)按事件傷害程度統(tǒng)計(jì)分析
2013年可疑醫(yī)療器械不良事件報(bào)告中,事件傷害為死亡的報(bào)告共75份,占總報(bào)告數(shù)的0.0003%;事件傷害為嚴(yán)重傷害的報(bào)告34,524份,占總報(bào)告數(shù)的14.5%;事件傷害為其他的報(bào)告共204,051份,占總報(bào)告數(shù)的85.5%(圖8)。
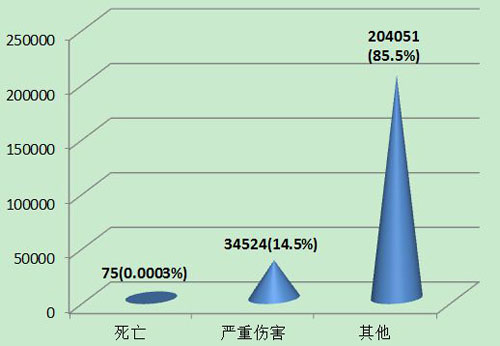
圖8 2013年醫(yī)療器械不良事件報(bào)告事件傷害程度情況
2013年,嚴(yán)重傷害事件報(bào)告數(shù)量及所占比例均比2012年有所增加。總體來(lái)看,可疑醫(yī)療器械不良事件的報(bào)告數(shù)量延續(xù)了2009年以來(lái)的增長(zhǎng)趨勢(shì),報(bào)告的質(zhì)量及信息的可利用程度等有了較大提升(圖9)。
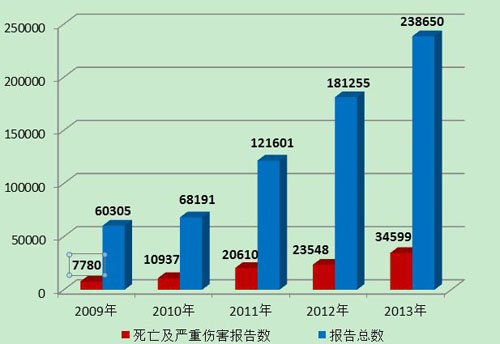
圖9 2009-2013年全國(guó)報(bào)告數(shù)量與死亡及嚴(yán)重傷害報(bào)告數(shù)量比較
(三)按醫(yī)療器械管理類別統(tǒng)計(jì)分析
2013年醫(yī)療器械不良事件報(bào)告中,涉及Ⅲ類醫(yī)療器械的報(bào)告最多,共105,032份(其中死亡及嚴(yán)重傷害事件報(bào)告22,416份),占總報(bào)告數(shù)的44.0%;涉及Ⅱ類醫(yī)療器械的報(bào)告次之,共80,394份(其中死亡及嚴(yán)重傷害事件報(bào)告9,157份),占總報(bào)告數(shù)的33.7%;涉及Ⅰ類器械的報(bào)告最少,共48,254份(其中死亡及嚴(yán)重傷害事件報(bào)告2,597份),占總報(bào)告數(shù)的20.2%;部分報(bào)告涉及的器械管理類別不詳,共4,970份報(bào)告(其中死亡及嚴(yán)重傷害事件報(bào)告429份),占報(bào)告總數(shù)的2.1%。Ⅱ類、Ⅲ類醫(yī)療器械的報(bào)告是構(gòu)成主體,與醫(yī)療器械風(fēng)險(xiǎn)程度高低相吻合(圖10,圖11)。
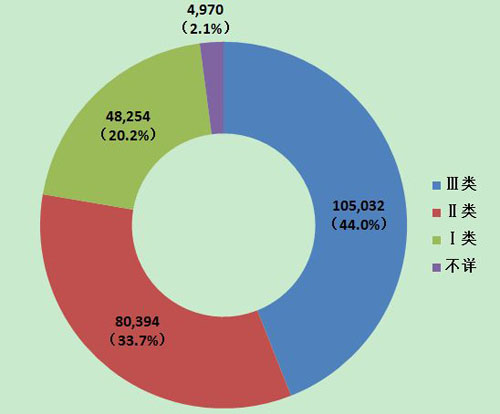
圖10 2013年醫(yī)療器械不良事件報(bào)告涉及產(chǎn)品管理類別情況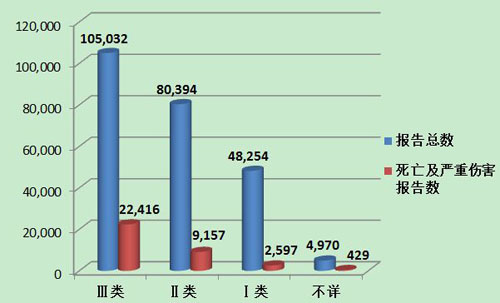
圖11 2013年死亡及嚴(yán)重傷害醫(yī)療器械不良事件報(bào)告涉及產(chǎn)品管理類別情況
(四)按醫(yī)療器械分類產(chǎn)品目錄統(tǒng)計(jì)分析
按照現(xiàn)行的《醫(yī)療器械分類目錄》,2013年的可疑醫(yī)療器械不良事件報(bào)告共涉及43類產(chǎn)品(除產(chǎn)品分類不詳或未填寫等其他外),涵蓋了《醫(yī)療器械分類目錄》中的所有醫(yī)療器械類別。其中,報(bào)告數(shù)量位列前十位的產(chǎn)品類別依次為醫(yī)用高分子材料及制品,注射穿刺器械,醫(yī)用衛(wèi)生材料及敷料,植入材料和人工器官,物理治療設(shè)備,醫(yī)用光學(xué)器具、儀器及內(nèi)窺鏡設(shè)備,普通診察器械,醫(yī)用電子儀器設(shè)備,手術(shù)室、急救室、診療室設(shè)備及器具和醫(yī)用縫合材料及粘合劑。與2012年相比,報(bào)告數(shù)量位列前十位的產(chǎn)品類別完全相同,僅排名略有變化(表2)。
表2 2013年醫(yī)療器械不良事件報(bào)告涉及產(chǎn)品分類目錄情況
| 序號(hào) |
分類 |
報(bào)告數(shù) |
構(gòu)成比(%) |
| 1 |
6866醫(yī)用高分子材料及制品 |
38413 |
16.1 |
| 2 |
6815注射穿刺器械 |
31589 |
13.2 |
| 3 |
6864醫(yī)用衛(wèi)生材料及敷料 |
30980 |
13.0 |
| 4 |
6846植入材料和人工器官 |
24912 |
10.4 |
| 5 |
6826物理治療設(shè)備 |
24639 |
10.3 |
| 6 |
6822醫(yī)用光學(xué)器具、儀器及內(nèi)窺鏡設(shè)備 |
13736 |
5.8 |
| 7 |
6820普通診察器械 |
9695 |
4.1 |
| 8 |
6821醫(yī)用電子儀器設(shè)備 |
7100 |
3.0 |
| 9 |
6854手術(shù)室、急救室、診療室設(shè)備及器具 |
6459 |
2.7 |
| 10 |
6865醫(yī)用縫合材料及粘合劑 |
4830 |
2.0 |
(五)按可疑醫(yī)療器械不良事件報(bào)告數(shù)量排名前五位產(chǎn)品統(tǒng)計(jì)分析
2013年可疑醫(yī)療器械不良事件報(bào)告中,報(bào)告數(shù)量排名前五位的無(wú)源醫(yī)療器械分別為一次性使用輸液器、宮內(nèi)節(jié)育器、一次性使用無(wú)菌注射器、角膜接觸鏡和靜脈留置針,占總報(bào)告數(shù)的34.0%,詳見(jiàn)表3。報(bào)告數(shù)量排名前五位的有源醫(yī)療器械分別為病人監(jiān)護(hù)儀、輸液泵和注射泵、電子血壓計(jì)、心電圖機(jī)和呼吸機(jī),占報(bào)告總數(shù)的4.3%,詳見(jiàn)表4。
表3 報(bào)告數(shù)量排名前五位的無(wú)源醫(yī)療器械
| 序號(hào) |
產(chǎn)品名稱 |
報(bào)告數(shù)(n) |
占報(bào)告總數(shù)的百分比(%) |
嚴(yán)重傷害報(bào)告數(shù) |
占本類產(chǎn)品報(bào)告數(shù)的百分比(%) |
| 1 |
一次性使用 輸液器 |
28824 |
12.1 |
2148 |
7.5 |
| 2 |
宮內(nèi)節(jié)育器 |
19822 |
8.3 |
9811 |
49.5 |
| 3 |
一次性使用無(wú)菌注射器 |
16517 |
6.9 |
823 |
5.0 |
| 4 |
角膜接觸鏡 |
8174 |
3.4 |
2201 |
26.9 |
| 5 |
靜脈留置針 |
7857 |
3.3 |
1198 |
15.2 |
| 合計(jì) |
81194 |
34.0 |
16181 |
- |
表4 報(bào)告數(shù)量排名前五位的有源醫(yī)療器械
| 序號(hào) |
產(chǎn)品名稱 |
報(bào)告數(shù)(n) |
占報(bào)告總數(shù)的百分比(%) |
嚴(yán)重傷害報(bào)告數(shù) |
占本類產(chǎn)品報(bào)告數(shù)的百分比(%) |
| 1 |
病人監(jiān)護(hù)儀 |
3761 |
1.6 |
742 |
19.7 |
| 2 |
輸液泵和注射泵 |
2708 |
1.1 |
539 |
19.9 |
| 3 |
電子血壓計(jì) |
2033 |
0.9 |
60 |
3.0 |
| 4 |
心電圖機(jī) |
942 |
0.4 |
120 |
12.7 |
| 5 |
呼吸機(jī) |
747 |
0.3 |
240 |
32.1 |
| 合計(jì) |
|
10191 |
4.3 |
1701 |
- |
(六)按涉及使用人員統(tǒng)計(jì)分析
2013年可疑醫(yī)療器械不良事件報(bào)告中,70.1%的報(bào)告所涉及的醫(yī)療器械是由專業(yè)人員操作的;2.2%的報(bào)告所涉及的醫(yī)療器械是由非本人的非專業(yè)人員操作的;11.2%的報(bào)告所涉及的醫(yī)療器械是由患者自己操作的;16.5%的報(bào)告操作人不詳。其中,由專業(yè)人員操作的報(bào)告所占比例與2012年相比基本持平(2012年,由專業(yè)人員操作的報(bào)告占報(bào)告總數(shù)的72.1%)。現(xiàn)有信息提示,操作人員是分析事件發(fā)生原因時(shí)要考量的重要因素之一,而報(bào)告操作人不詳所占比例偏大,提示報(bào)告質(zhì)量仍有待提高(圖12)。
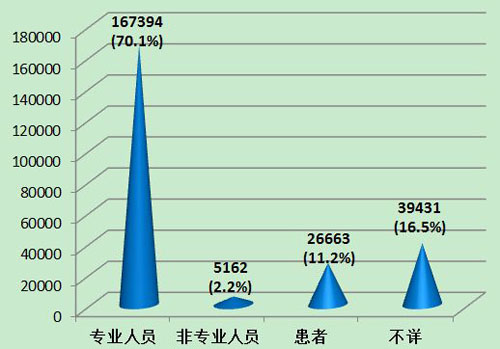
圖12 2013年醫(yī)療器械不良事件報(bào)告涉及使用人員情況
(七)按涉及實(shí)際使用場(chǎng)所統(tǒng)計(jì)分析
2013年可疑醫(yī)療器械不良事件報(bào)告中,使用場(chǎng)所為“醫(yī)療機(jī)構(gòu)”的報(bào)告161,871份,占67.8%;使用場(chǎng)所為“家庭”的報(bào)告共37,855份,占15.9%;使用場(chǎng)所為“其他”(如體驗(yàn)中心等)的報(bào)告共9,625份,占4.0%;使用場(chǎng)所為“不詳”的報(bào)告共29,299份,占12.3%。醫(yī)療器械的使用場(chǎng)所呈現(xiàn)多元化的趨勢(shì),使用場(chǎng)所的復(fù)雜性也是分析不良事件發(fā)生原因時(shí)需要考量的因素之一(圖13)。
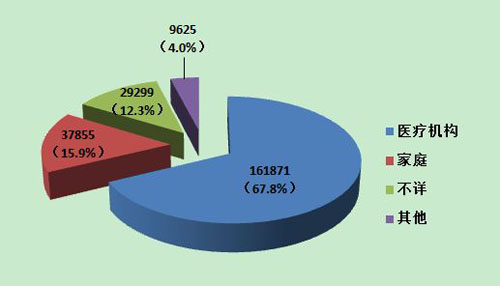
圖13 2013年醫(yī)療器械不良事件報(bào)告涉及實(shí)際使用場(chǎng)所情況
三、對(duì)醫(yī)療器械安全性問(wèn)題采取的主要措施情況
(一)發(fā)布《醫(yī)療器械不良事件信息通報(bào)》
2013年,共發(fā)布《醫(yī)療器械不良事件信息通報(bào)》3期,涉及接骨板、人工髖關(guān)節(jié)、醫(yī)用電子直線加速器三個(gè)產(chǎn)品(表4-1)。
接骨板的臨床使用風(fēng)險(xiǎn)主要表現(xiàn)為:鋼板斷裂、彎曲、松動(dòng),排異反應(yīng)、異常疼痛、骨折不愈合、感染等。風(fēng)險(xiǎn)控制建議:生產(chǎn)企業(yè)應(yīng)重視產(chǎn)品的不良事件監(jiān)測(cè),開(kāi)展分析和再評(píng)價(jià),進(jìn)一步提高產(chǎn)品性能,加強(qiáng)質(zhì)量控制,并對(duì)臨床醫(yī)務(wù)人員提供必要的技術(shù)支持和培訓(xùn)。臨床醫(yī)務(wù)人員應(yīng)嚴(yán)格掌握手術(shù)適應(yīng)癥及禁忌癥,選擇適當(dāng)規(guī)格型號(hào)的產(chǎn)品;嚴(yán)格按照說(shuō)明書和手術(shù)規(guī)范的要求進(jìn)行操作;③規(guī)范術(shù)前術(shù)后對(duì)病人的管理。
人工髖關(guān)節(jié)的臨床使用風(fēng)險(xiǎn)主要表現(xiàn)為:假體松動(dòng)、斷裂、周圍感染,關(guān)節(jié)脫位,術(shù)后疼痛,假體骨水泥植入綜合征等。風(fēng)險(xiǎn)控制建議:生產(chǎn)企業(yè)應(yīng)改進(jìn)產(chǎn)品設(shè)計(jì),進(jìn)一步提高產(chǎn)品性能,提高生產(chǎn)工藝,選擇生物相容性好、耐磨損、剛度適宜的材料,加強(qiáng)質(zhì)量控制;提供詳盡的標(biāo)簽及使用說(shuō)明書,并對(duì)臨床醫(yī)務(wù)人員提供必要的技術(shù)支持和培訓(xùn)。臨床醫(yī)務(wù)人員應(yīng)嚴(yán)格掌握關(guān)節(jié)置換的適應(yīng)癥及禁忌癥;加強(qiáng)業(yè)務(wù)培訓(xùn),嚴(yán)格按照說(shuō)明書和手術(shù)規(guī)范的要求進(jìn)行操作;規(guī)范術(shù)后護(hù)理;加強(qiáng)人工關(guān)節(jié)置換準(zhǔn)入制度的管理,加強(qiáng)驗(yàn)收、儲(chǔ)存、使用控制,建立詳細(xì)的使用記錄。
醫(yī)用電子直線加速器的臨床使用風(fēng)險(xiǎn)主要表現(xiàn)為:放射治療引發(fā)的并發(fā)癥(白細(xì)胞、血小板減少、脫發(fā)、放射性皮炎、非照射部位炎癥、惡心、嘔吐、腹脹、腹瀉等。以及機(jī)械故障、電氣故障、和軟件故障等。風(fēng)險(xiǎn)控制建議:生產(chǎn)企業(yè)應(yīng)完善售后產(chǎn)品技術(shù)支持,提高產(chǎn)品可靠性;加強(qiáng)對(duì)臨床醫(yī)務(wù)人員的培訓(xùn);對(duì)常見(jiàn)設(shè)備故障,應(yīng)與臨床共同探討,提出改進(jìn)措施。醫(yī)務(wù)人員應(yīng)嚴(yán)格掌握放射治療的適應(yīng)征,按照相關(guān)規(guī)章制度及說(shuō)明書要求維護(hù)、操作、使用電子直線加速器,制定科學(xué)合理治療方案。
原文鏈接:
http://www.cdr.gov.cn/xxtb_255/ylqxblsjxxtb/
(二)發(fā)布《醫(yī)療器械警戒快訊》
2013年,共發(fā)布《醫(yī)療器械警戒快訊》10期,共71條安全性信息,涉及體外除顫儀、呼吸機(jī)、麻醉機(jī)、人工關(guān)節(jié)、血糖監(jiān)測(cè)儀、腹膜透析管、電動(dòng)輪椅、計(jì)算機(jī)斷層掃描圖像處理工作站等產(chǎn)品。
(三)召開(kāi)產(chǎn)品專家分析會(huì)及產(chǎn)品企業(yè)溝通會(huì)
2013年,總局、國(guó)家中心共召開(kāi)了4次醫(yī)療器械產(chǎn)品專家分析會(huì)、1次產(chǎn)品生產(chǎn)經(jīng)營(yíng)企業(yè)溝通會(huì)。
專家分析會(huì)涉及的產(chǎn)品為接骨板、人工髖關(guān)節(jié)、醫(yī)用電子直線加速器和制氧機(jī)。會(huì)議對(duì)產(chǎn)品相關(guān)的安全性事件及可疑不良事件報(bào)告進(jìn)行了討論分析,并針對(duì)產(chǎn)品常見(jiàn)風(fēng)險(xiǎn)點(diǎn)提出了風(fēng)險(xiǎn)控制意見(jiàn),采取了風(fēng)險(xiǎn)控制措施。
企業(yè)溝通會(huì)涉及的產(chǎn)品為殼聚糖。國(guó)家中心針對(duì)殼聚糖相關(guān)產(chǎn)品的不良事件監(jiān)測(cè)情況及使用中存在的安全性問(wèn)題組織召開(kāi)了企業(yè)溝通會(huì)。生產(chǎn)企業(yè)代表介紹了其產(chǎn)品的概況及不良事件收集與處置情況。會(huì)議對(duì)殼聚糖類產(chǎn)品的風(fēng)險(xiǎn)及可能原因進(jìn)行了分析,并提出了風(fēng)險(xiǎn)控制建議。
醫(yī)療器械不良事件監(jiān)測(cè)小貼士
1.醫(yī)療器械:是指直接或者間接用于人體的儀器、設(shè)備、器具、體外診斷試劑及校準(zhǔn)物、材料以及其他類似或者相關(guān)的物品,包括所需要的計(jì)算機(jī)軟件;其效用主要通過(guò)物理等方式獲得,不是通過(guò)藥理學(xué)、免疫學(xué)或者代謝的方式獲得,或者雖然有這些方式參與但是只起輔助作用;其目的是:
(1)疾病的診斷、預(yù)防、監(jiān)護(hù)、治療或者緩解;
(2)損傷的診斷、監(jiān)護(hù)、治療、緩解或者功能補(bǔ)償;
(3)生理結(jié)構(gòu)或者生理過(guò)程的檢驗(yàn)、替代、調(diào)節(jié)或者支持;
(4)生命的支持或者維持;
(5)妊娠控制;
(6)通過(guò)對(duì)來(lái)自人體的樣本進(jìn)行檢查,為醫(yī)療或者診斷目的提供信息。
2.醫(yī)療器械不良事件:指獲準(zhǔn)注冊(cè)或已備案、質(zhì)量合格的醫(yī)療器械,在正常使用情況下發(fā)生的,導(dǎo)致或可能導(dǎo)致人體傷害的各種有害事件。
根據(jù)醫(yī)療器械不良事件的危害程度和發(fā)生的原因,醫(yī)療器械生產(chǎn)企業(yè)必要時(shí)應(yīng)當(dāng)采取警示、檢查、修理、重新標(biāo)簽、修改說(shuō)明書、軟件升級(jí)、替換、收回、銷毀等控制措施。
目前,我國(guó)醫(yī)療器械不良事件監(jiān)測(cè)按照“可疑即報(bào)”原則收集報(bào)告,即為可疑醫(yī)療器械不良事件報(bào)告。
3.醫(yī)療器械不良事件監(jiān)測(cè):是指對(duì)醫(yī)療器械不良事件的發(fā)現(xiàn)、報(bào)告、調(diào)查、評(píng)價(jià)和控制的過(guò)程。
4.嚴(yán)重醫(yī)療器械不良事件:指有下列情況之一者:
(1)導(dǎo)致死亡;
(2)危及生命;
(3)導(dǎo)致機(jī)體功能的永久性傷害或者機(jī)體結(jié)構(gòu)的永久性損傷;
(4)必須采取醫(yī)療措施才能避免上述永久性傷害或者損傷;
(5)由于醫(yī)療器械故障、可用性等問(wèn)題可能導(dǎo)致上述所列情況的。
5.醫(yī)療器械不良事件與質(zhì)量事故、醫(yī)療事故的區(qū)別
(1)醫(yī)療器械不良事件主要是由于產(chǎn)品的設(shè)計(jì)缺陷、已經(jīng)注冊(cè)審核的使用說(shuō)明書不準(zhǔn)確或不充分等原因造成的,但其產(chǎn)品的質(zhì)量是合格的。
(2)醫(yī)療器械質(zhì)量事故主要是指其質(zhì)量不符合注冊(cè)產(chǎn)品標(biāo)準(zhǔn)等規(guī)定造成的事故。
(3)醫(yī)療事故是指醫(yī)療機(jī)構(gòu)及其醫(yī)務(wù)人員在醫(yī)療活動(dòng)中,違反醫(yī)療衛(wèi)生管理法律、行政法規(guī)、部門規(guī)章和診療護(hù)理規(guī)范、常規(guī),過(guò)失造成患者人身?yè)p害的事故。(摘自衛(wèi)生部《醫(yī)療事故處理?xiàng)l例》)








